开发
mRNA生产
稳定性研究
生成
mRNA生产
QC分析
工艺开发
我们可以为不同靶向性(肝、脾)、不同制剂形式(冷冻剂型、冻干剂型)的mRNA-LNP提供GMP生产工艺流程的开发及优化。
菌种三级建库
GMP条件下的高稳定性三级建库,提供建库报告、传代稳定性分析、全面的质检标准。自主知识产权的菌种具有高传代稳定性、高传代倍数的PolyA尾丢失率<10%。
质粒工艺开发
稳定、可靠的发酵和纯化工艺,可达到高纯(>90%)、低杂、重组率<5%、高产量,工艺开发过程完整、记录清晰可追溯。全套分析方法:超螺旋比例、重组率、质粒拷贝数、活菌数、宿主DNA /RNA/蛋白残留、测序、卡那霉素残留、微限、内毒素等 。
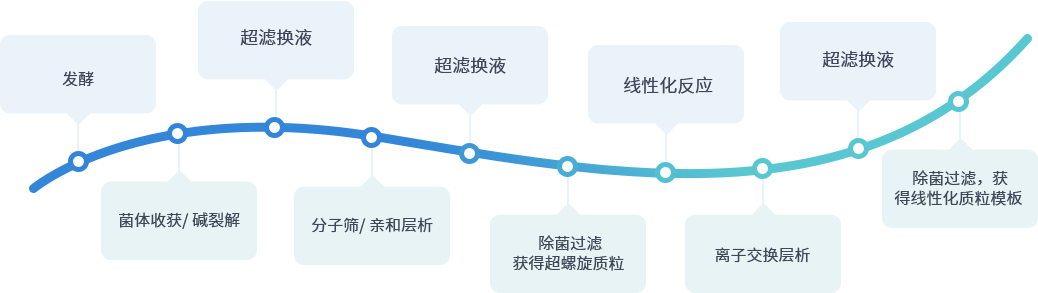

原液工艺开发
结合高保真T7聚合酶,可控的dsRNA含量。稳定、可靠的IVT和纯化工艺,高纯、低杂、高产量、工艺完整、记录清晰可追溯。纯度>90%,加帽率 >90%,双链残留≤1μg/mg mRNA。
全套原液相关质检方法:mRNA纯度(CE、HPLC)、加帽率、测序、polyA尾长、dsRNA含量、总蛋白残留、模板残留、体内活性研究、体外活性研究、微限、内毒素等。


制剂工艺开发
稳定、可靠的制备及纯化工艺,高包封率、可控粒径、分散性小、工艺完整、记录清晰可追溯。冷冻制剂可在<-60°C保存超2年。包封率>85%,粒径 <150 nm。
依诺特色制剂冻干工艺,可满足不同mRNA及LNP组合冻干需求,制剂2-8°C储运效期>2年,室温储运效期>1年。使用前复溶即可,方便快捷,可及性高。包封率>80%,粒径<150 nm。
全套制剂相关质检方法:mRNA含量、包封量、粒径、电位、解离常数、微观形态、mRNA纯度、脂质含量和鉴别、水分、内毒素、无菌、乙醇残留、柠檬酸残留、体内外生物学活性分析、纳米流式分析(空载率、核酸拷贝数)等。






工艺相关检定项目及方法
| 样品类型 | 项目类型 | 检验项目 | 方法名称 |
| 菌种库相关检定 | 菌种的生物学活性检查 | 菌落形态 | 划种LB琼脂平板法 |
| 培养特征 | 麦康凯琼脂培养基 | ||
| 革兰氏染色镜检 | 显微镜法 | ||
| 生化反应 | IMVic试验和糖发酵试验 | ||
| 培养物纯度 | 显微镜法 | ||
| 抗生素抗性 | 培养法 | ||
| 活菌数 | 涂布平板法 | ||
| 污染检查 | 电镜检查 | 透射电镜法 | |
| 噬菌体 | 双层平板法 | ||
| 菌种序列鉴定 | 全基因序列测序 | 二代和三代结合测序法 | |
| 质粒特性确认 | 目的基因序列测定 | 一代测序法 | |
| 质粒酶切图谱 | 电泳法 | ||
| 超螺旋率 | 提取质粒+HPLC法 | ||
| poly(A)尾稳定性 | PCR法+电泳法 | ||
| 质粒产量 | UV法 | ||
| 质粒丢失率 | 培养法 | ||
| 质粒拷贝数 | qPCR法 | ||
| 质粒DNA相关检定 | 理化特性 | 外观 | 目测法 |
| pH值 | 酸度计法 | ||
| 含量 | 质粒DNA含量、纯度(A260/280) | 紫外分光光度法 | |
| 质粒DNA含量 | HPLC法 | ||
| 鉴别 | 基因序列 | 测序法 | |
| 酶切图谱 | 琼脂糖凝胶电泳 | ||
| 纯度 | 电泳纯度 | 琼脂糖凝胶电泳 | |
| 超螺旋比例 | HPLC法 | ||
| 线性化比例 | HPLC法 | ||
| 杂质检测 | 卡那霉素残留 | 酶联免疫吸附法 | |
| 宿主蛋白残留 | 酶联免疫吸附法 | ||
| 宿主DNA残留 | Q-PCR法 | ||
| 宿主RNA残留 | Q-PCR法 | ||
| 总蛋白残留 | NanoOrange | ||
| 安全性检测 | 微生物限度 | 薄膜过滤法 | |
| 细菌内毒素 | 光度法 | ||
| mRNA原液相关检定 | 理化特性 | 外观 | 目测法 |
| PH值 | 酸度计法 | ||
| 含量 | mRNA 紫外含量 | UV法 | |
| 鉴别 | mRNA 序列一致性 | 测序法 | |
| mRNA 序列长度 | CE法 | ||
| mRNA紫外吸收峰 | UV法 | ||
| 纯度 | mRNA 紫外纯度 | UV法 | |
| mRNA纯度 | SEC-HPLC法 | ||
| mRNA 纯度 | CE法 | ||
| mRNA纯度 | 琼脂糖凝胶电泳 | ||
| 加帽率 | RP-LC-MS法 | ||
| poly(A)尾长度 | RP-LC-MS法 | ||
| 杂质检测 | 双链RNA残留 | ELISA法 | |
| 总蛋白残留 | NanoOrange 法 | ||
| DNA模版残留 | Q-PCR法 | ||
| 乙醇残留 | 康卫血法 | ||
| 活性检测 | 体外生物活性 | 细胞转染+WB+Elisa | |
| 安全性检测 | 无菌检查 | 薄膜过滤法 | |
| 细菌内毒素检查 | 光度测定法 | ||
| LNP-mRNA制剂相关检定 | 理化特性 | 外观 | 目测法 |
| pH值 | 酸度计法 | ||
| 可见异物 | 灯检法 | ||
| 装量差异 | 称重法 | ||
| 渗透压摩尔浓度 | 冰点下降法 | ||
| 不溶性微粒 | 光阻法 | ||
| 鉴别 | mRNA序列一致性 | 测序法 | |
| 脂质鉴别 | RP-HPLC-CAD | ||
| 含量 | mRNA含量及包封率 | 荧光染料法 | |
| 脂质含量 | RP-HPLCCAD | ||
| 蔗糖含量 | HPLC-RID | ||
| 纯度 | mRNA纯度及序列长度 | CE法 | |
| mRNA纯度 | HPLC法 | ||
| 杂质检测 | LNP各组分游离脂质含量 | HPLC-CAD | |
| 水分 | 费休氏法 | ||
| 乙醇残留 | 康卫血扩散法 | ||
| 生物活性检测 | 体外生物学活性 | 细胞转染+WB+Elisa | |
| 体内生物学活性 | 结合抗体滴度 | ||
| 安全性检测 | 无菌检查 | 薄膜过滤法 | |
| 细苗内毒素检查 | 光度法 | ||
| LNP表征 | 纳米颗粒大小和分散系数 | 动态光散射法 | |
| LNP微观形态 | Cryo -TEM | ||
| 空壳率/RNA拷贝数 | 纳米流式 |
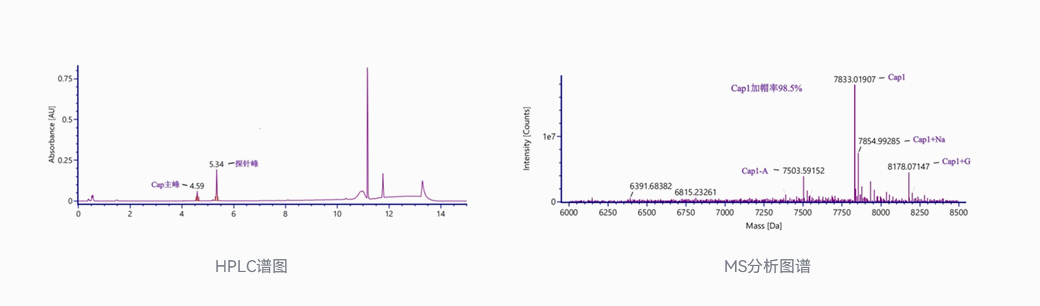
加帽率检测
使用LC-MS法检测加帽率,可以根据产物分子量精准定位uncapped产物、capped产物(cap1 、cap1-A、cap1+G),计算各产物的响应值和占比得到加帽率,是公认的加帽率准确的检测方法。其方法原理是设计特异性的探针与mRNA 5'端序列配对结合,使用RNase H酶对结合后的5'端特异位点进行酶切(酶切位置可能会出现-A或者+G的位移),使用磁珠纯化后,上机LC-MS。HPLC可以实现mRNA的Cap主峰与探针的分离,MS(Q-Tof检测器)可以对Cap主峰的各产物分离定量。分析uncapped峰和capped峰的占比,可以计算得到产品的加帽率。依诺生物的mRNA产品均具有极高的加帽率。
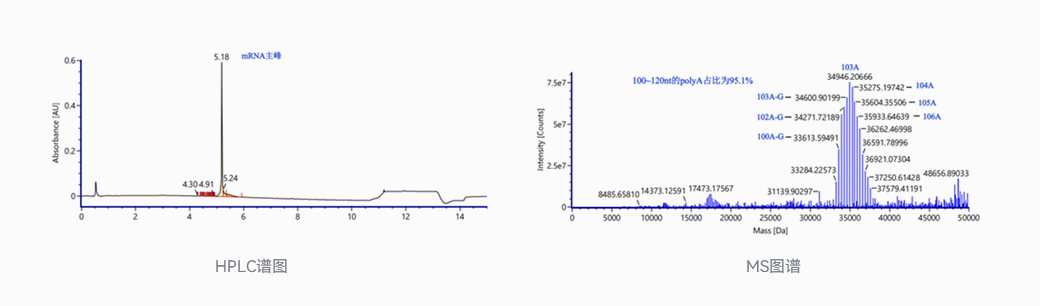
PolyA尾展示
使用LC-MS法检测mRNA产品polyA尾的分布,可以根据产物分子量,可以精准定位到1个nt的长度差别,计算不同长度的polyA尾的响应值和占比,可以得到整体polyA尾的分布情况,是目前polyA尾最优的检测方法。其方法原理是设计特异性的探针与mRNA 3'端序列配对结合,使用RNase H酶对结合后的3'端特异位点进行酶切(酶切位置可能会出现-G的位移),使用磁珠纯化后,上机LC-MS。HPLC可以实现mRNA的polyA尾主峰与探针的分离,MS(Q-Tof检测器)可以对mRNA的polyA尾主峰的各产物分离定量。根据分子量精准定位,可以分析得到不同序列长度的polyA尾的占比。依诺生物的mRNA产品,polyA尾长度高度集中在设计长度。
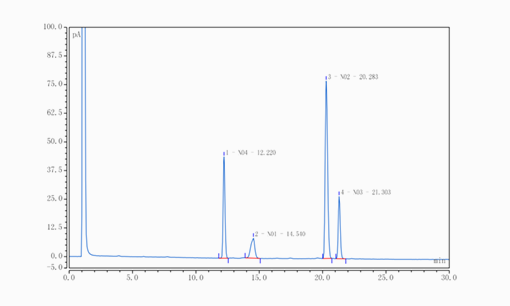
mRNA-LNP各脂质组分含量及游离脂质含量检测
使用UHPLC-CAD和C18色谱柱,在同一色谱条件下,可以实现LNP四种脂质组分的有效分离,经过与标准品的比较,可以有效定量mRNA-LNP各脂质组分含量及游离脂质含量,表征mRNA-LNP的关键质量属性。
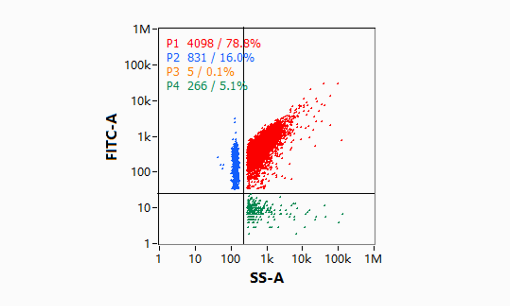
纳米流式仪
纳米流式原理类似细胞流式仪,可实现单个纳米颗粒(7-1000 nm)高通量检测。通过侧散射光(side scatter, SS)信号可获得LNP的数目和分散情况。使用SYTO9荧光染料可以标记样品内所有mRNA,结合SS信号,可以区分游离mRNA和完整mRNA-LNP,进而计算样品单个LNP颗粒平均核酸拷贝数、包封率和空载率。上图为依诺样品的纳米流式分析图,核酸拷贝数为3.3,包封率较高,为94.2%,空壳率较低,为4.7%,说明样品中的有效mRNA-LNP占比数量较高,空载杂质低。
依诺生物专业团队,拥有10余年mRNA专业研发经验,并已成功推动mRNA传染病疫苗、mRNA药物在多个国家和地区获批开展临床试验。依诺生物的专家团队可提供一体化解决方案,覆盖mRNA产业链的全部环节,依托公司运营多年的IPD体系,为客户提供优质的服务。




